Unser Körper ist voller unsichtbarer Schalter. Auf der Oberfläche jeder Zelle sitzen Millionen winziger Empfänger, sogenannte Rezeptoren, die Signale aus der Umgebung aufnehmen und weitergeben. Funktionieren diese Schalter nicht richtig, können Krankheiten entstehen, von Krebs bis zu neurologischen Erkrankungen. Ein Forschungsteam der Universität Leipzig hat jetzt einen zentralen Mechanismus bei einer besonderen Gruppe solcher Empfänger entschlüsselt.
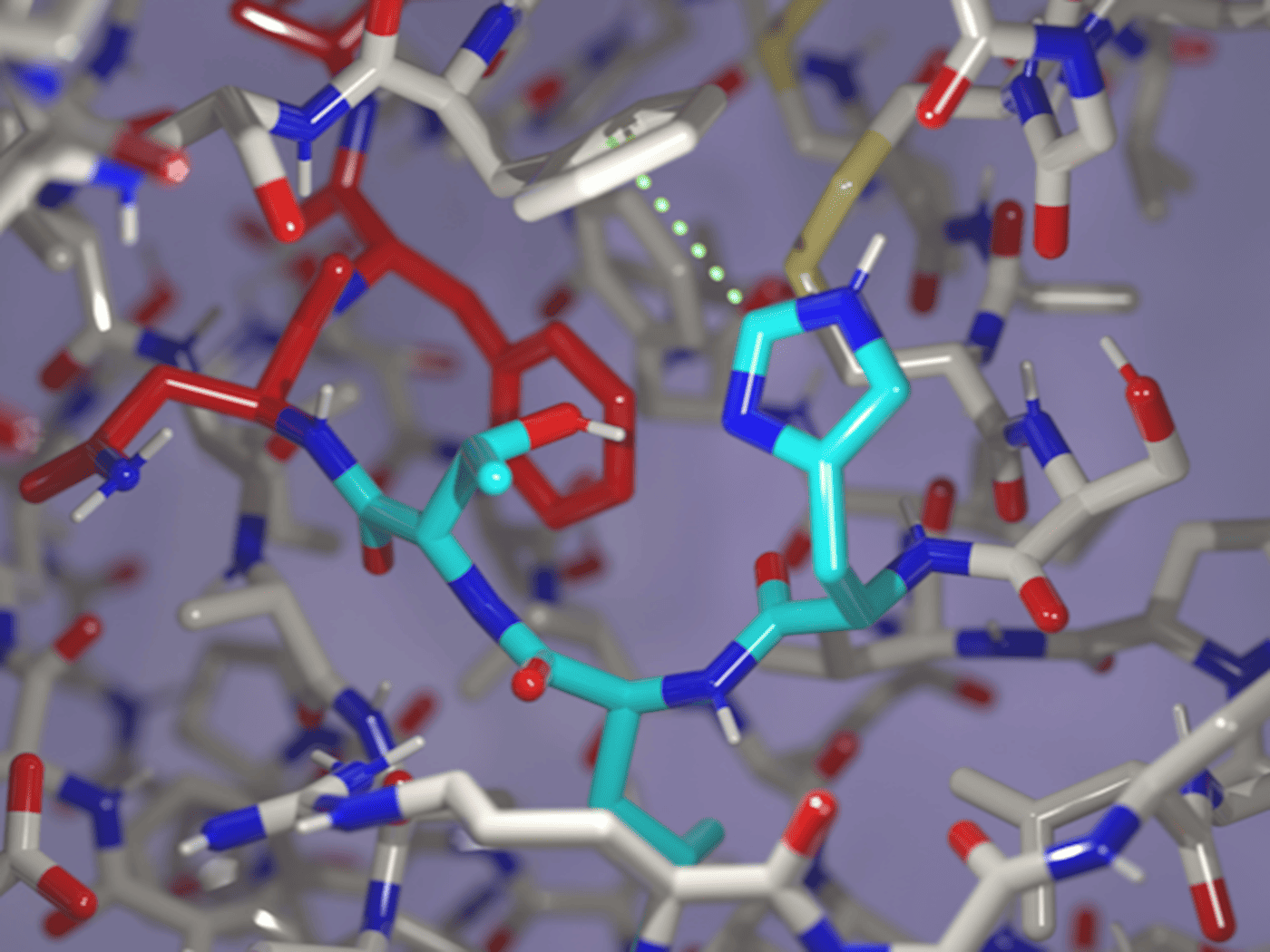
Im Mittelpunkt stehen die sogenannten Adhäsions-G-Protein-gekoppelten Rezeptoren (aGPCRs). Diese Eiweiß-Strukturen sitzen an der Zelloberfläche und messen unter anderem mechanische Kräfte, etwa wenn Zellen miteinander in Kontakt treten. Sie gehören zu einer Proteinfamilie, über die rund ein Drittel aller Medikamente wirkt, sind selbst aber bislang kaum therapeutisch genutzt. Sie haben ein besonderes Merkmal: Sie können sich selbst spalten. Dabei trennt sich ein Abschnitt des Proteins in zwei Teile. Ein Schritt, der den Rezeptor aktiviert. Doch warum die Selbstspaltung bei manchen Rezeptoren kaum stattfindet, war bisher unklar.
Neue Behandlungsansätze möglich
Auf dieser Grundlage griffen die Forschenden gezielt ein. Sie veränderten bewegliche Bereiche des Proteins und ergänzten die fehlende Aminosäure. Die Spaltung lief nun plötzlich in weniger als zwei Tagen ab statt in 100. "Unsere Ergebnisse zeigen, dass die Spaltung von Adhäsions-GPCRs nicht nur von der chemischen Sequenz, sondern auch von der Struktur und Proteindynamik abhängt", sagt Prof. Dr. Norbert Sträter vom Institut für Bioanalytische Chemie. Das sei ein entscheidender Schritt, um zu verstehen, wie diese Rezeptoren aktiviert werden und wie man sie gezielt beeinflussen könnte.
Zugleich zeigte die Studie, dass manche dieser Rezeptoren sogar ganz ohne Spaltung funktionieren. Langfristig könnten die Erkenntnisse zu neuen Behandlungsansätzen bei Krebs, Entzündungskrankheiten und Erkrankungen des Nervensystems führen.
Originalpublikation:
Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026).